文献解读
项目论文|磁珠多位点对磷酸化肽段高效富集的分析研究-Nanoscale-201810
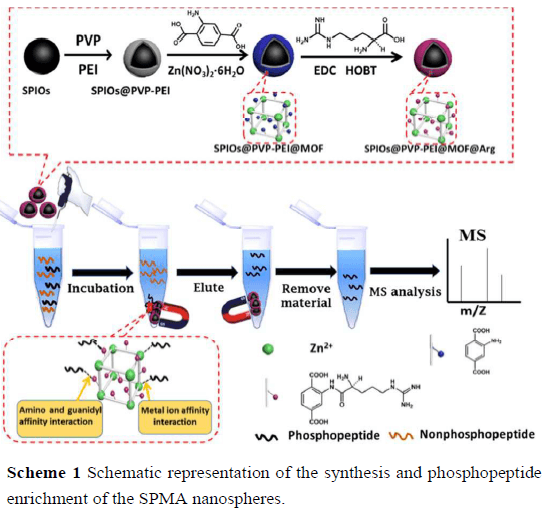
可逆蛋白磷酸化是最普遍的翻译后蛋白修饰之一,在调节许多生物学过程中起着重要作用。由于它参与多种疾病(例如癌症和阿尔茨海默氏病)的发现和探索,磷酸化蛋白和磷酸肽非常重要。近年来,质谱(LC-MSMS)已成为分析蛋白质磷酸化的最通用和最强大的工具,但是,由于动态化学计量低,质量差,鉴定和表征复杂生物样品中的低丰度磷酸肽仍然是一项挑战。电离效率高,信号抑制严重。因此,从复杂的生物样品中高效选择性地捕获和富集磷酸肽对于质谱分析极为重要。目前已有多种用于富集磷酸肽的技术,特别是固定化的金属离子亲和色谱(IMAC)和金属氧化物亲和色谱(MOAC)。不幸的是,这些方法遭受金属阳离子损失(IMAC)和繁琐且耗时的制备过程(MOAC)的困扰。基于金属中心和磷酸基团之间相互作用强度的差异,MOAC材料趋于富集单磷酸肽,而IMAC材料对多磷酸肽的选择性更高。实际上,富集包括单和多磷酸肽在内的全磷酸肽对于磷酸蛋白质组分析至关重要。具有多亲和位点的磁性胍基功能化的金属-有机框架纳米球,其中多亲和位点由由氧化锌基于MOAC方法和特异性识别基团(氨基和胍基)组成,被合成出来,合成策略是结合了对磁性氨基衍生的MOF外延生长和合成后修饰方法,该纳米球对全磷酸化肽段的高效富集展现出巨大的潜力。


材料:六水合氯化铁(III),六水合硝酸锌,二氧化钛微球,胰蛋白酶
 目的:为了提高全磷酸肽富集的效率,多种材料和串联洗脱方法的组合是常见的策略,多步操作和顺序洗脱程序面临着低水平磷酸肽丢失的风险。有报道称以金属为中心的双锆有机骨架与MOAC和固定的IMAC结合使用,具有改善全磷酸肽富集效率的潜力。本文作者受到将MOAC和IMAC结合在单一材料上的策略的启发,多个亲和位点的概念将为材料平台提供具有多个特定的公认分子,以提高整体磷酸肽富集的效率。
目的:为了提高全磷酸肽富集的效率,多种材料和串联洗脱方法的组合是常见的策略,多步操作和顺序洗脱程序面临着低水平磷酸肽丢失的风险。有报道称以金属为中心的双锆有机骨架与MOAC和固定的IMAC结合使用,具有改善全磷酸肽富集效率的潜力。本文作者受到将MOAC和IMAC结合在单一材料上的策略的启发,多个亲和位点的概念将为材料平台提供具有多个特定的公认分子,以提高整体磷酸肽富集的效率。
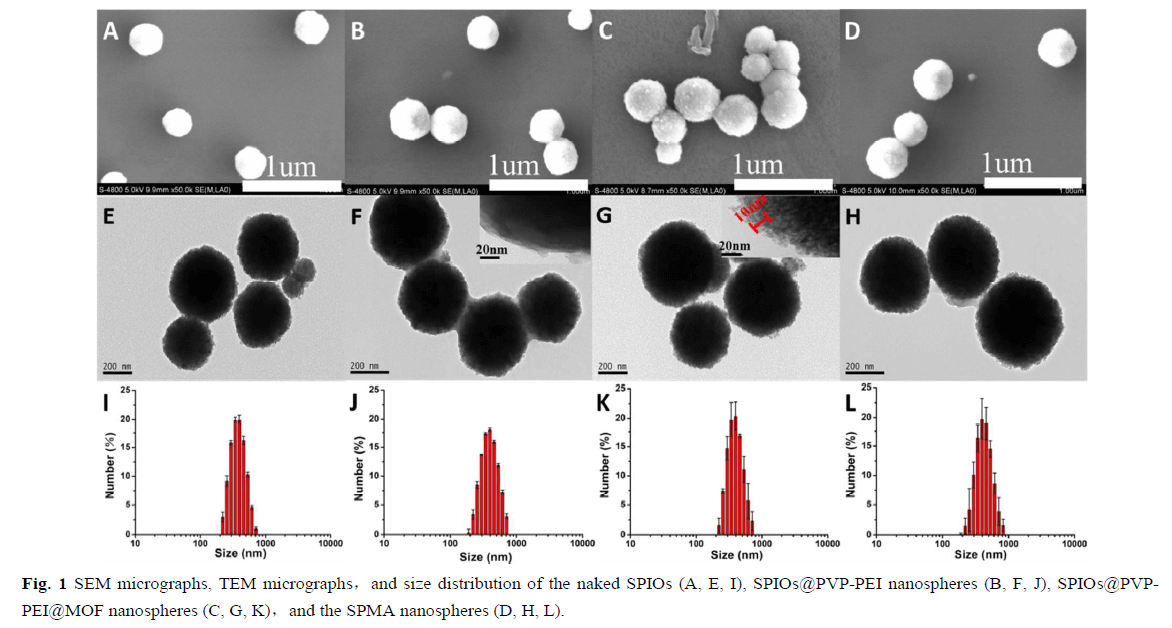
实验:作者将合成出的材料SPMA纳米球通过扫描电子显微镜(SEM)和透射电子显微镜(TEM)图像如Fig.1所示。SPIO,SPIOs@PVP-PEI纳米球,SPIO@PVP-PEI@MOF纳米球和SPMA纳米球均具有均匀的 球形形态和良好的单分散性(Fig.1(AH))。由于PVP/PEI涂层,SPIOs@PVP-PEI纳米球的表面很光滑。用MOFs固定后,清楚地观察到约10nm的晶体状。(Fig.1(F,G))。接枝的精氨酸对SPMA纳米球的形态和大小没有明显影响(Fig.1(C,D,G,H))。同时,动态光散射(DLS)表明水中SPIOs,SPIOs@PVP-PEI纳米球,SPIOs@PVP-PEI@MOF纳米球和SPMA纳米球的平均直径分别为337.3±5.1nm,345.7±10.2nm,360.6±14.3nm和365.3±15.8nm。这些与SEM和TEM观察结果一致(Fig.1(I-L))。
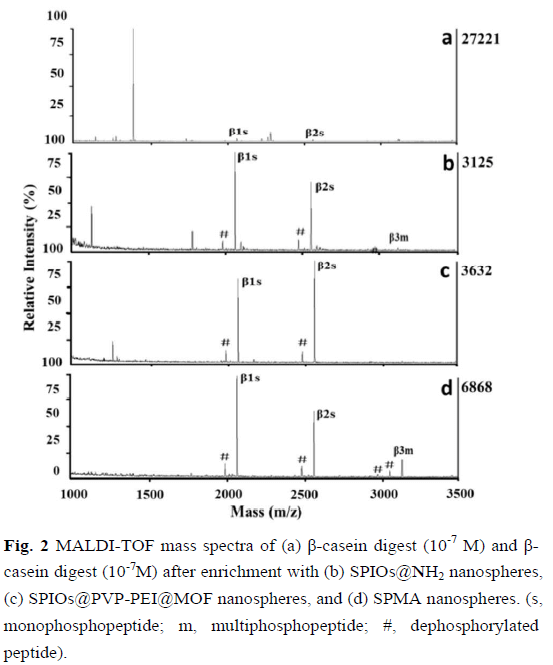
为了证明全球磷酸肽富集的多亲和力位点的优越性,作者设计了SPIOs@NH2纳米球(包括NH2基团)和SPIOs@PVP-PEI@MOF纳米球(包括ZnO簇和NH2基团)作为对照。通过MALDI-TOF MS,使用不同的亲和材料富集之前和之后的β-酪蛋白胰蛋白酶消化物(10-7M)。Fig.2显示了几个未磷酸化的峰和单磷酸肽(β1s,β2s),而用SPIOs@NH2纳米球和SPIOs@PVP-PEI@MOF纳米球处理后,多磷酸肽(β3m)的质谱信号强度极低。相反,在富含SPMA纳米球后,整体磷酸肽的峰占据了光谱的大部分,没有非磷酸化的峰。这些结果表明,SPMA纳米球的多亲和力位点(Zn-O簇,NH2基团和胍基基团)可以协同作用引起全磷酸肽的高选择性富集。选择性富集全磷酸肽的原因可以解释如下。由于电离效率较低,单磷酸肽会严重抑制多磷酸肽的MS信号,单磷酸肽会竞争性占据亲和位点(Zn-O团簇和NH2基团)。因此,SPIOs@NH2纳米球(包括NH2基团)和SPIOs @ PVP-PEI @ MOF纳米球(包括Zn-O簇和NH2基团)几乎不能富集多磷酸肽。然而,磷酸肽的胍基和磷酸基可形成盐桥结构。它具有带(-)(+)(-)或(+)(-)(+)的带电基团排列的静电相互作用。盐桥结构可以提供强大的非共价相互作用,并抵消了单磷酸肽和多磷酸肽。因此,SPMA纳米球(包括胍基)可以同时富集单和多磷酸肽。
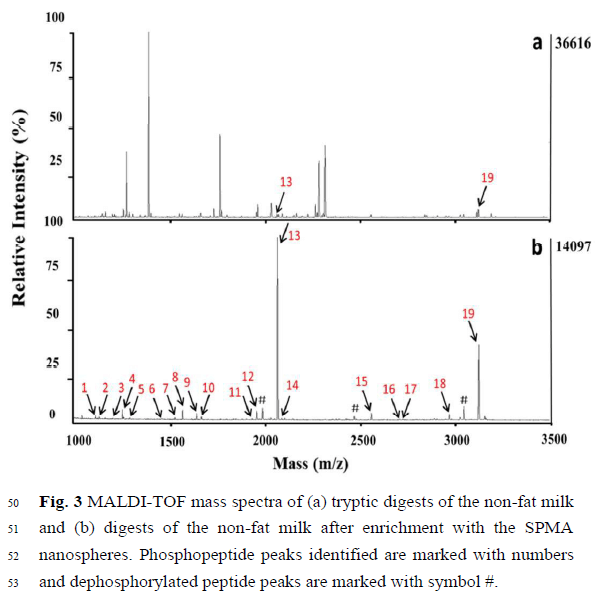
为了检验富集策略在实际生物环境中的实际应用,将SPMA纳米球用于捕获复杂程度更高的脱脂牛奶消化物中的磷酸肽,几乎所有非磷酸肽和磷酸肽的两个弱峰出现在脱脂牛奶消化(Fig.3)。用SPMA纳米球处理后,可以确定地鉴定出强度很高的19种磷酸肽,并具有清晰的背景。相反,SPIOs@PVP-PEI@MOF纳米球和SPIOs@NH2纳米球也用于脱脂牛奶消化物中的磷酸肽富集。结果表明,SPMA纳米球对实际样品中的磷酸肽具有较高的选择性。
为了进一步评估在实际应用中的潜力,将SPMA纳米球用于从大鼠脑裂解液的复杂胰蛋白酶消化物中富集磷酸肽,然后使用LC-MSMS分析,鉴定出1659个独特的磷酸肽。此外,由SPMA纳米球鉴定的单和多磷酸肽的数量分别为1606(96.8%)和53(3.2%)。这些结果表明,SPMA纳米球显示出从复杂混合物中富集全球磷酸肽的良好性能,并在磷酸化蛋白质组学研究中具有巨大潜力。
结论:多亲和位点的磁性胍基功能化的金属-有机框架纳米球,用于富集全球磷酸肽。 这些SPMA纳米球具有结构稳定性,出色的磁响应性,并且可以通过简单的合成方法来形成。模拟复合物样品和真实生物样品中的磷酸肽的富集表明SPMA纳米球在高选择性富集全磷酸肽方面具有出色的性能。 更重要的是,提供了一种通用方法来指导亲和材料的设计,以提高整体磷酸肽,甚至糖肽富集的效率。